Infektionsblockade als frühestmögliche antivirale Maßnahme
Ludwig: Neben diesen Virus-gerichteten Entwicklungen gibt es zunehmend innovative Ansätze, die nicht mehr auf das Virus selbst, sondern auf die Wirtszelle abzielen. Viren sind zellobligate Parasiten und benötigen für ihre Vermehrung in vielfältiger Weise zwingend die Funktionen Ihrer Wirtszelle. Durch Behandlung der Wirtszelle mit Wirkstoffen, die solche Funktionen beeinträchtigen, ist es also möglich, die Virusfunktion wie auch die Virusvermehrung zu hemmen. Vorteil der Behandlung ist, dass das Virus nicht die Möglichkeit besitzt, durch Anpassung die beeinträchtigten zellulären Funktionen zu ersetzen und somit ist die Bildung von Resistenzen weitestgehend ausgeschlossen.
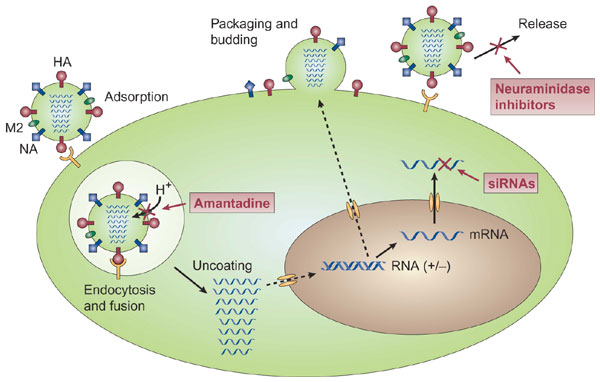
© Nature Medicine, 2004
Abbildung: Der lange Weg des Virus von der Zellinfektion bis zur Freisetzung bietet viele Möglichkeiten der prophylaktischen und therapeutischen Interaktion
Hier nutzt man zunächst neuste Erkenntnisse über die Interaktion zellulären Faktoren mit viralen Proteinen, beispielsweise des Polymerasekomplex oder des viralen Nichtstrukturproteins, um blockierende Substanzen zu finden, die diese für das Virus essentielle Interaktion unterbrechen. In gleicher Weise werden Inhibitoren präklinisch erprobt, welche die Bindung und Fusion viraler und zellulärer Membranen während der Virusaufnahme blockieren.
ine weitere Strategie ist die Inhibition von bestimmten Enzymen oder Signalwegen, die das Virus essentiell benötigt, um sich zu vermehren. Als Beispiel seine hier Inhibitoren von zellulären Signalkaskaden, wie der Raf/MEK/ERK Kinasekaskade oder des IKK/NF-kappaB Moduls, genannt. Der MEK Inhibitor U0126 oder der NF-kappaB Inhibitor SC75741 führen beide zu einer effizienten Hemmung der Influenzavirus-Vermehrung in Zellkultur und im Tierexperiment, ohne schädlich für die Wirtszelle zu sein oder resistente Varianten zu erzeugen. Ein weiterer großer Vorteil dieser Substanzen ist, dass sie neben der direkten Wirkung auf die virale Vermehrung auch indirekt durch die Beeinflussung einer überschießenden zellulären Zytokinantwort wirken können und so diese vor allem bei Infektionen mit hochpathogenen Influenzaviren vorkommende Komplikation vermeiden helfen. Darüber hinaus befinden sich viele Inhibitoren der entsprechenden Signalwege für andere Indikationen bereits in klinischer Erprobung und könnten für die Indikation Grippe relativ leicht weiterentwickelt werden.
Das viel versprechende Gebiet zellulärer Angriffspunkte für die anti-Influenzatherapie steht dabei erst am Anfang seiner Entwicklung und es wird derzeit in verschiedenen umfangreichen Screeningansätzen nach weiteren zellulären Faktoren gefahndet, die das Virus benötigt, um sich effektiv zu vermehren.
Autor
• Rainer H. Bubenzer, Heilpflanzen-Welt (2008).